Xantotoxina
| Xantotoxina | |
| Identificación | |
|---|---|
| Nombre IUPAC | 9-m "toxi-7H-furo [3,2-g] cromen-7-ona |
| Sinónimos |
xantotoxina, metoxsaleno, 8-metoxipsoraleno |
| N o CAS | |
| N o ECHA | 100,005,516 |
| N o EC | 206-066-9 |
| N o RTECS | LV1400000 |
| Código ATC |
D05 D05 |
| DrugBank | DB00553 |
| PubChem | 3971 |
| Sonrisas |
COc1c2c (ccc (= O) o2) cc3c1occ3 , |
| InChI |
InChI: InChI = 1 / C12H8O4 / c1-14-12-10-8 (4-5-15-10) 6-7-2-3-9 (13) 16-11 (7) 12 / h2- 6H, 1H3 InChIKey: QXKHYNVANLEOEG-UHFFFAOYAV Est. InChI: InChI = 1S / C12H8O4 / c1-14-12-10-8 (4-5-15-10) 6-7-2-3-9 (13) 16-11 (7) 12 / h2- 6H, 1H3 Est. InChIKey: QXKHYNVANLEOEG-UHFFFAOYSA-N |
| Propiedades químicas | |
| Fórmula bruta |
C 12 H 8 O 4 [Isómeros] |
| Masa molar | 216.1895 ± 0.0114 g / mol C 66.67%, H 3.73%, O 29.6%, |
| Propiedades físicas | |
| T ° fusión | 148 hasta 150 ° C |
| Solubilidad | 47,6 mg · l -1 (agua, 30 ° C ) |
| Precauciones | |
| SGH | |
  H302, H334, P261, P342 + P311,
H302 : Nocivo en caso de ingestión
H302, H334, P261, P342 + P311,
H302 : Nocivo en caso de ingestión H334 : Puede provocar síntomas de alergia o asma o dificultades respiratorias si se inhala P261 : Evite respirar el polvo / humo / gas / niebla / vapores / aerosoles. P342 + P311 : Si experimenta síntomas respiratorios: llame a un CENTRO DE INFORMACIÓN TOXICOLÓGICA oa un médico. |
|
| Ecotoxicologia | |
| DL 50 |
423 mg · kg -1 (ratón, oral ) 860 mg · kg -1 (ratón, sc ) 250 mg · kg -1 (ratones, ip ) |
| LogP | 2.140 |
| Datos farmacocinéticos | |
| Vida media de elimin. | ~ 2 horas |
| Unidades de SI y STP a menos que se indique lo contrario. | |
La xantotoxina o metoxsaleno (vendido bajo los nombres de Oxsoralène , Deltasoralène , Meladinine , UVADEX ) es un compuesto orgánico de la familia de las furocumarinas . Es el derivado 8-metoxilado del psoraleno . Se utiliza como tratamiento para determinadas enfermedades de la piel.
Ocurrencia natural
La xantotoxina está presente de forma natural en una planta medicinal africana, el fagarier ( Fagara xanthoxyloïdes ), así como en muchas plantas de la familia de las umbelíferas , en particular el ammi alto ( Ammi majus ) de donde se extrae, la angélica , la chirivía , el perejil gigante , o de la familia Rutaceae como la bergamota .
Biosíntesis
La xantotoxina se produce por una ruta específica, la ruta de las furocumarinas lineales que permiten formar furocumarinas como el psoraleno y sus derivados a partir de la umbeliferona , ella misma biosintetizada según la ruta de los fenilpropanoides , y del pirofosfato de dimetilalilo , obtenido a través del mevalonato .
Síntesis de umbeliferona
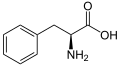
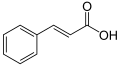
La umbeliferona es una cumarina , una de las muchas subfamilias de fenilpropanoides y, por lo tanto, se biosintetiza como esta última a partir de L-fenilalanina de acuerdo con la vía de los fenilpropanoides (o vía del shikimato ). La fenilalanina se convierte en primer lugar en ácido cinámico por la acción de la fenilalanina amoniaco liasa (PAL), esta última luego se hidroxila en ácido paracumarico por la acción de la cinamato 4-hidroxilasa (C4H). Este último es nuevamente hidroxilado por la acción de cinamato / cumarato 2-hidroxilasa (C2H) para formar ácido 2,4-dihidroxicinámico , luego por una rotación del enlace insaturado adyacente al grupo carboxilo de este último. La reacción termina con la esterificación intramolecular, el grupo hidroxilo C2 'es atacado por el grupo carboxilo, formando un anillo de lactona .


Síntesis de xantotoxina
La biosíntesis continúa luego a través de la activación de pirofosfato de dimetilalilo (DMAPP), producido por la vía del mevalonato, que forma un carbocatión por escisión del difosfato. Una vez activada, la enzima umbeliferona 6-preniltransferasa cataliza la C-alquilación entre DMAPP y umbeliferona a la posición activada, orto al fenol, lo que lleva a la formación de demetilsuberosina. Esta reacción es seguida por una hidroxilación catalizada por la enzima marmesina sintasa que forma la marmesina , seguida de una segunda hidroxilación con salida de acetona catalizada por la psoraleno sintasa que forma el psoraleno . A continuación, el psoraleno se transforma mediante la acción de psoraleno 8-monooxigenasa formando xantotoxol . Este último ve su grupo fenol metilado por reacción con S-adenosilmetionina , una reacción catalizada por xantotoxol O-metiltransferasa que forma xantotoxina.
Tratamiento de enfermedades de la piel.
Debido a su capacidad fotosensibilizante de la piel (que comparte con otras furocumarinas), la xantotoxina se utiliza, junto con la exposición de la piel al sol, como fármaco en el tratamiento de enfermedades de la piel como psoriasis , eccema o vitiligo y contra ciertos linfomas cutáneos. La xantotoxina cambia la forma en que las células de la piel reciben los rayos UV-A , lo que suprimiría la enfermedad. Generalmente se prescribe una dosis de 10 mg de xantotoxina antes de un tratamiento con PUVA ( psoraleno + UV-A) de 30 mg / 75 minutos.
Riesgos
Las personas con presión arterial alta o antecedentes de problemas hepáticos tienen riesgo de inflamación y daño irreversible al hígado y la piel. Los efectos secundarios incluyen náuseas , dolor de cabeza , mareos y, en casos raros, insomnio .
La xantotoxina es tóxica para los animales de sangre fría .
Notas y referencias
- masa molecular calculada de " pesos atómicos de los elementos 2007 " en www.chem.qmul.ac.uk .
- hoja de Sigma Aldrich , consultado el 15 de junio, 2011
- (en) " xantotoxina " en ChemIDplus , consultado el 15 de junio de, 2 011
- Drogas and Chemical Toxicology. Vuelo. 2, pág. 309, 1979
- Drogas en Japón Vol. 6, pág. 837, 1982
- Alfa Aesar 15 de junio de 2011 , consultado en
- biosíntesis de furanocumarina lineal
- PM Dewick , Productos medicinales naturales: un enfoque biosintético , John Wiley & Sons ,2009, 3 e ed. , p. 161, 164–165
- (fr) Este artículo está tomado parcial o totalmente del artículo de Wikipedia en inglés titulado " Methoxsalen " ( ver la lista de autores ) .



