Prolina
| Prolina | |
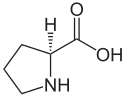 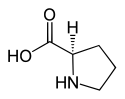 L o S (-) - prolina y D o R (+) - prolina |
|
| Identificación | |
|---|---|
| Nombre IUPAC | pirrolidina ácida -2- carboxílico |
| Sinónimos |
P, Pro |
| N o CAS |
(racémico) (L) oS(-) (D) oR(+) |
| N o ECHA | 100,009,264 |
| N o CE | 205-702-2 (L) |
| FEMA | 3319 |
| Sonrisas |
[H] N1CCCC1C (O) = O , |
| InChI |
InChI: InChI = 1 / C5H9NO2 / c7-5 (8) 4-2-1-3-6-4 / h4,6H, 1-3H2, (H, 7,8) |
| Propiedades químicas | |
| Fórmula bruta |
C 5 H 9 N O 2 [Isómeros] |
| Masa molar | 115,1305 ± 0,0054 g / mol C 52,16%, H 7,88%, N 12,17%, O 27,79%, |
| pKa | 1,95 - 10,64 |
| Propiedades bioquimicas | |
| Codones | CCA , CCU , CCG , CCC |
| pH isoeléctrico | 6.30 |
| Aminoácido esencial | No |
| Ocurrencia en vertebrados | 5,0% |
| Precauciones | |
| WHMIS | |
|
Producto incontroladoEste producto no está controlado de acuerdo con los criterios de clasificación de WHMIS. |
|
| Unidades de SI y STP a menos que se indique lo contrario. | |
La prolina (Abreviaturas IUPAC - IUBMB : Pro y P ) es un ácido α-amino ácido cuyo enantiómero L es uno de los 22 aminoácidos proteinógenos , codificada en el ARN mensajero por el codones CCU, CCC, CCA y CCG. Es el único aminoácido proteinogénico que tiene una amina secundaria y no primaria , lo que le confiere una geometría particular que tiende a interrumpir las estructuras secundarias de proteínas como las hélices α y las láminas β .
La prolina forma residuos apolares que, en la polimerización, pueden formar varios tipos de proteínas en una familia llamada poliprolinas .
La presencia de muchos residuos de prolina puede ser el origen de una hélice de prolina; este es particularmente el caso del colágeno . El ciclo de la prolina es casi plano. Esto se puede demostrar considerando los ángulos de enlace en este anillo.
En el mundo animal
La prolina participa en particular en la síntesis de colágeno, que tiene la secuencia ( Gly –Pro– Hyp ) n y cicatrices.
En el mundo vegetal
La prolina participa en la germinación adecuada de las semillas, la floración y otras fases del desarrollo de las plantas.
Se han observado acumulaciones de prolina en muchas especies de plantas cuando se exponen a varios tipos de estrés ambiental.
Un creciente cuerpo de evidencia apoya una correlación positiva entre estas acumulaciones y el manejo metabólico de estas tensiones por parte de las plantas. Tiene un papel osmolito, pero también es un quelante de metales y tiene propiedades antioxidantes. “Aplicado de forma exógena y en dosis bajas, mejora la tolerancia al estrés en las plantas”, pero varios saltadores también han notado efectos adversos en dosis más altas.
Datos
- Fuerza Van der Waals : 90
- pK1 (α-COOH): 1,95
- pK2 (αN-H): 10,64
La prolina contiene en su molécula una función amina secundaria cíclica.
Otro aminoácido, la hidroxiprolina , se deriva de la prolina por 4- hidroxilación .
Notas y referencias
- masa molecular calculada de " pesos atómicos de los elementos 2007 " en www.chem.qmul.ac.uk .
- (en) Francis A. Carey, " Tabla de valores de pK y pH " , en el Departamento de Química de la Universidad de Calgary , 2014(consultado el 26 de julio de 2015 )
- (en) Mr. Beals, L. Gross, S. Harrell, " Amino Acid Frequency " en The Institute for Environmental Modeling (ITSH) de la Universidad de Tennessee (consultado el 26 de julio de 2015 )
- " Proline (l-) " en la base de datos de productos químicos Reptox de la CSST (organización de Quebec responsable de la seguridad y salud en el trabajo), consultado el 25 de abril de 2009
- J. Behre, R. Voigt, I. Althöfer, S. Schuster: Sobre la importancia evolutiva del tamaño y planaridad del anillo de prolina . Naturwissenschaften 99 (2012) 789-799.
- (en) Mudasir Irfan Dar , Mohd Irfan Naikoo , Farha Rehman , Fauzia Naushin y Fareed Ahmad Khan , “Proline La acumulación en plantas: Roles en la tolerancia al estrés y el desarrollo de la planta” , en Noushina Iqbal, Rahat Nazar y Nafees Un Khan, Osmolytes and Plants Aclimation to Changing Environment: Emerging Omics Technologies , Nueva Delhi, Springer,2016( ISBN 978-81-322-2615-4 y 978-81-322-2616-1 , DOI 10.1007 / 978-81-322-2616-1_9 ) , pág. 155-166.
Ver también
Bibliografía
- Ali Q, Ashraf M, Athar HUR (2007) La prolina aplicada de forma exógena en diferentes etapas de crecimiento mejora el crecimiento de dos cultivares de maíz cultivados en condiciones de déficit de agua. Pak J Bot 39: 1133-1144
- (en) Patrick Armengaud , Laurent Thiery , Nathalie Buhot y Ghislaine Grenier-de March , “ La regulación transcripcional de la biosíntesis de prolina en Medicago truncatula revela características específicas del desarrollo y el medio ambiente ” , Physiologia Plantarum , vol. 120, n o 3,Marzo de 2004, p. 442–450 ( ISSN 0031-9317 y 1399-3054 , DOI 10.1111 / j.0031-9317.2004.00251.x , leído en línea , consultado el 21 de octubre de 2020 )
- (en) M. Ashraf y MR Foolad , " Funciones de la glicina betaína y la prolina en la mejora de la resistencia al estrés abiótico de las plantas " , Botánica experimental y ambiental , vol. 59, n o 2Marzo de 2007, p. 206–216 ( DOI 10.1016 / j.envexpbot.2005.12.006 , leído en línea , consultado el 21 de octubre de 2020 )