Aldehído
Un aldehído es un compuesto orgánico , perteneciente a la familia de los compuestos carbonílicos , uno de los átomos de carbono primario (conectado a un máximo de un átomo de carbono) de la cadena de carbono lleva un grupo carbonilo. Por tanto, un aldehído contiene la secuencia:
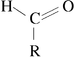 (R representa una cadena de carbono).
(R representa una cadena de carbono).
El aldehído más simple (R reducido a un solo átomo de H) es el formaldehído (o metanal ), también llamado formalina cuando está en solución acuosa:
Un aldehído se deriva formalmente de un alcohol primario ( oxidación ) en el que el grupo hidróxido -OH está al final de la cadena y se forma tras la eliminación de dos átomos de H, de ahí el nombre " al cool de s hyd rogéné" o aldehído .
Nomenclatura
El aldehído tendrá el nombre del alcano correspondiente, al que se le añade el sufijo "-al". Por lo demás, las reglas son las mismas que las establecidas para los alquenos . Cuando el aldehído es el grupo funcional prioritario de la molécula, no es necesario asignarle un índice posicional, ya que siempre está en la posición terminal (1).
CH 3 - CHO: etanal
CH 3 - CH (CH 3 ) - CH 2 - CHO: 3-metilbutanal
Cuando el aldehído es un sustituyente de un compuesto cíclico como el benceno , entonces lleva el nombre de carbaldehído o carboxaldehído, que son dos términos equivalentes. Por ejemplo, el siguiente compuesto puede llamarse bencenocarbaldehído o bencenocarboxaldehído ( también se acepta el nombre común benzaldehído ):
C 6 H 5 - CHO
Cuando el grupo aldehído no es una prioridad, se le asigna un prefijo de la forma alcanoílo . Por ejemplo, el siguiente compuesto se llama ácido etanoilbencenosulfónico :
OHC - CH 2 - C 6 H 5 - SO 3 H
Aldehídos principales
| Metanal | Ethanal | Propanal | Butanal | Pentanal |
| VSH 2 O | C 2 H 4 O | C 3 H 6 O | C 4 H 8 O | C 5 H 10 O |
Propiedades, reactividad
Generalmente son comunes a los aldehídos y cetonas (ver características del compuesto de carbonilo ).
Producción y síntesis
Por hidroformilación
También llamado proceso oxo , esta reacción se usa para obtener aldehídos C 3 -C 19de los alquenos, es el proceso principal para la producción de butanal . Se emplea monóxido de carbono y dihidrógeno a una presión de 10 a 100 atmósferas y una temperatura de 40 a 200 ° C en presencia de un catalizador (un metal de transición como el rodio ).
Por oxidación de alcoholes
Los aldehídos se obtienen por oxidación de alcoholes primarios y cetonas por oxidación de alcoholes secundarios (el alcohol terciario solo puede oxidarse en condiciones extremas, a menudo se considera no oxidable).
Por lo tanto, esta oxidación involucra al par redox:
Sin embargo, los aldehídos siguen siendo buenos agentes reductores. Por tanto, se oxidan muy fácilmente a ácidos carboxílicos :
Incluso hay un caso en el que la reacción continúa: metanol. Se oxida primero a metanal, luego a ácido metanoico y finalmente a dióxido de carbono.
- oxidación por O 2 del aire
Catalizador se puede usar como Fe 2 O 3 o MnO 3 a 400 ° C , o un catalizador de plata a 600 ° C .
- Deshidrogenación catalítica de alcoholes primarios
El alcohol es carbonatado. CuO alrededor de 400 a 500 ° C , Ag, Cu alrededor de 300 ° C , ZnO o ZrO $ alrededor de 300 a 400 ° C se utiliza como catalizador .
- Un método de Hoechst-Wacker
Oxidación de etileno a acetaldehído
Oxidación químicaSe debe utilizar un oxidante "suave", bajo estrictas condiciones de funcionamiento, para evitar la segunda oxidación. En general, se utiliza un derivado de cromo VI en proporciones estequiométricas. Hay 2 métodos históricos:
- Para los aldehídos de cadena carbonada corta y, por tanto, más volátiles, se utiliza dicromato de potasio K 2 Cr 2 O 7 , en medio ácido, a una temperatura superior al punto de ebullición del aldehído, lo que permite su extracción después del entrenamiento.
- Para los otros aldehídos, se hace uso de reactivo de Sarett, compuesto de cromo VI trióxido de CrO 3 en piridina , a baja temperatura ( 0 ° C ).
Sin embargo, los compuestos de piridina y cromo son muy tóxicos y ya no se pueden usar. Se han desarrollado otros métodos:
- El PCC y PDC, siempre a base de cromo, pero en menor cantidad;
- Métodos de DMSO activado (incluida la oxidación de Swern );
- Periodados (reactivos de Dess-Martin , IBX).
Por ozonólisis de alquenos
Los aldehídos se pueden obtener mediante ozonólisis de alquenos. Es importante utilizar un aditivo reductor durante la reacción, como un sulfuro (convencionalmente dimetilsulfuro) o una fosfina (trifenilfosfina, menos olorosa que los compuestos de azufre), para atrapar los subproductos oxidantes (peróxido de hidrógeno). De lo contrario, se observa una sobreoxidación del aldehído a ácido carboxílico .
usar
Los aldehídos son productos sintéticos muy potentes que aportan, independientemente de su propio olor, un prodigioso poder de difusión a las composiciones. En perfumería, se trata principalmente de aldehídos alifáticos. El descubrimiento de los aldehídos dio a los creadores una nueva paleta. Su marcado uso está en el origen de los perfumes del tipo llamado "Aldehído". Los aldehídos se utilizan como medio de desinfección y en la fabricación de preparados orgánicos. Los aldehídos y cetonas se utilizan en la fabricación de plásticos, disolventes, tintes, perfumes y medicamentos. Por ejemplo, el aldehído C 17 tiene olor a cereza.
Acetalización
La acetalización es una reacción reversible para transformar un compuesto carbonílico y dos alcoholes (o diol) en acetal . Esta reacción en realidad protege al grupo carbonilo o al alcohol.
Reacción- Calentador
- Catálisis ácida (generalmente APTS )
- Cuando se utiliza un aldehído, el producto obtenido se denomina "acetal". Cuando se utiliza una cetona, el producto obtenido se denomina "cetal". Sin embargo, cada vez más se utiliza el término acetal como término genérico para designar los 2 productos. Por otro lado, la reacción (tanto para aldehídos como para cetonas) siempre se denomina "acetalización".
- Esta reacción es generalmente a favor del acetal (a diferencia de los cetales).
Si queremos potenciarlo en esta dirección, utilizamos un exceso de alcohol (que a la vez sirve como disolvente), también podemos destilar el agua (destilación heteroazeotrópica) utilizando el aparato de Dean y Stark . Para favorecer la reacción inversa, es todo lo contrario: ponemos un exceso de agua para hidrolizar el acetal.
- Cuando queremos proteger la función carbonilo, usualmente usamos un diol, como etano-1,2-diol :
- Esta reacción también puede servir muy bien para proteger una función del alcohol, en particular los dioles vecinales .
- En algunos casos, la reacción puede detenerse con el hemiacetal (caso de hemiacetales cíclicos).
Acción de un reactivo de Grignard
Un reactivo de Grignard reacciona con un aldehído para formar un alcohol secundario (→ reacción ).
Reacción de Wittig
La reacción de Wittig transforma un aldehído en un derivado de etileno. En realidad, convierte el enlace C = O en un enlace C = C.
Reducción de aldehídos
En alcoholes IndustrialmenteLa usado dihidrógeno H 2 en un disolvente inerte en presencia de un catalizador ( catálisis heterogénea ). Con mucha frecuencia se trata de metales, como platino (Pt), paladio (Pd), níquel (Ni) o rodio (Rh). Si alguna vez el aldehído también tiene un enlace C = C, este también se hidrogena (la reacción es más fácil en C = C que en C = O). la reacción es exotérmica .
Por hidrurosDIBAL se puede utilizar para la reducción de aldehídos a alcohol.
En alcanoPruebas de reconocimiento
Para demostrar la presencia de aldehído, podemos hacer una prueba de reconocimiento:
- Adición de compuestos de tipo Z-NH 2 (amina): formación de un precipitado.
- La prueba a la solución de Fehling que toma un rojo ladrillo en presencia de aldehído.
- La llamada prueba del " espejo de plata ", que utiliza el reactivo de Tollens, da como resultado la creación de un depósito de plata sólida.
- Prueba de reactivo de Schiff , que cuando está frío, colorea la solución de rosa.
Pero estos métodos que utilizan reacciones químicas con el aldehído lo destruyen. Los métodos de espectrometría (RMN e infrarrojos) que permiten detectar esta función sin destruir la muestra se utilizan ahora con mayor facilidad.